Povrchová ochrana
Povrchová ochrana  Možnosti spracovania salmiakového steru vznikajúceho v procese mokrého žiarového zinkovania
Možnosti spracovania salmiakového steru vznikajúceho v procese mokrého žiarového zinkovaniaMožnosti spracovania salmiakového steru vznikajúceho v procese mokrého žiarového zinkovania
Rubrika: Povrchová ochrana
V procese mokrého kusového žiarového zinkovania v oddelenej časti vane na povrchu roztaveného zinku dochádza k tvorbe špecifického odpadu – salmiakového steru. Tento odpad vzniká v dôsledku reakcií tavidla so zinkom, oxidom zinku a železom. Po určitom čase zinkovania, tavidlo tvorené NH4Cl stráca svoju aktivitu, funkciu a musí byť z hladiny roztaveného zinku odstránené. Podľa vyhlášky MŽP SR 284/2001 Z.z., ktorou sa ustanovuje Katalóg odpadov sa salmiakový ster zaraďuje medzi „nebezpečný odpad“ [1]. Aj napriek skutočnosti, že tento nebezpečný odpad obsahuje značné množstvo zinku končí v súčasnosti na skládke odpadov. Cieľom tohto príspevku je uviesť možné spôsoby spracovania salmiakového steru.
CHARAKTERISTIKA SALMIAKOVÉHO STERU A MOŽNOSTI JEHO SPRACOVANIA
Pri mokrom spôsobe zinkovania sa na hladine roztaveného zinku v oddelenej časti vane nachádza napenené tavidlo. Zinkovanie oceľových dielcov sa vykonáva práve v tejto časti vane, kedy výrobky ešte mokré z procesu morenia vstupujú do roztaveného zinku cez vrstvu tavidla.
Primárnym cieľom tavidla je rozpúšťať povrchové oxidy tvoriace sa na oceli po morení a aktivovať povrch ocele pred procesom tvorby povlaku. Dokonalé očistenie povrchu oceľových dielcov od oxidov železa a hrdze pred zinkovaním, zabezpečí dokonalú reakciu medzi roztaveným zinkom a železom, čo má za následok vytvorenie rovnomerného zinkového povlaku. Tavidlo okrem „čistiacej funkcie“ zabezpečuje tvorbu tenších povlakov, redukuje oxidáciu povrchu roztaveného zinku, redukuje tvorbu popola a ovplyvňuje tvorbu plynov [2–4].
Pri tomto type žiarového zinkovania je tavidlo tvorené NH4Cl s malým prídavkom peniaceho činidla – glycerínu. Prídavok peniaceho činidla prispieva k dosiahnutiu požadovanej hrúbky tavidla, ktorá pozitívne vplýva na jeho správnu funkciu a aktivitu [5]. Hlavná zložka tavidla (NH4Cl) sa v priebehu zinkovania stráca jednak odparovaním ale aj reakciami medzi zinkom, oxidom zinku a železom. Obsah chloridu amónneho (NH4Cl) v napenenom tavidle závisí od teploty (obr. 1).
Ako možno vidieť na obr. 1 s klesajúcou teplotou od rozhrania zinok/tavidlo smerom nahor stúpa percentuálne množstvo NH4Cl v tavidle, čo má za následok jeho nadmerné odparovanie. Obrázok 1, znázorňuje rovnovážne koncentrácie chloridu amónneho pre dané teploty. Tieto koncentrácie sa pohybujú v rozmedzí od 2 % do viac ako 30 %.Túto skutočnosť potvrdzuje aj (obr. 2), na ktorom je zobrazený fázový vzťah chloridu zinočnatého a chloridu amónneho v tavidlových systémoch [6].
Z uvedeného (obr. 2) vyplýva, že pri typickej teplote zinkovania t.j. 450 °C, maximálne množstvo NH4Cl, ktoré bude rozpustené v roztavenom ZnCl2 je len 2 až 3 %. Väčšie množstvá NH4Cl sa odparia až pokiaľ koncentrácia v tavenine nedosiahne rovnovážnu úroveň 2 – 3%. Pre správnu funkciu tavidla by sa obsah rozpusteného NH4Cl mal pohybovať v rozmedzí 10 – 15%. Táto koncentrácia sa dá dosiahnuť redukciou teploty, posúvaním sa pozdĺž rovnovážnej čiary smerom k vyšším obsahom NH4Cl v roztavenom tavidle [6]. Množstvo NH4Cl, ktoré zostane v roztavenom tavidle závisí od teploty. V priebehu zinkovania dochádza k procesu, kedy sa tavidlo obohacuje
o ZnCl2 tzv. zinkové maslo pričom dochádza k úbytku NH4Cl. Vtedy, tavidlo stráca svoje vlastnosti a musí byť z hladiny roztaveného zinku odstránené [6]. Odstraňovanie sa uskutočňuje v časových intervaloch (približne každé 4 – 8 hod.), pričom sťahovanie musí byť dôsledné, aby sa minimalizovalo zachytenie zinku v salmiakovom stere.
Salmiakový ster podľa autorov Kunhalmi [7], Krištofová [8] pozostáva z chloridu amónneho, oxidov, sulfidov a Zn. Okrem pôvodných solí: NH4Cl, ZnCl2 a Zn-Cl2.2NH4Cl, obsahuje aj 18 – 22 % Zn v kovovej forme, 30 – 35% ZnO a nečistoty hlavne Fe2O3. Sjoukes [9] uvádza, že chemické zloženie salmiakových sterov je: 48,1 % ZnCl2; 5,6 % Zn v kovovej forme; 27,4 % ZnO; 3,1 % chloridy hliníka a iné chloridy, oxidy hliníka, železa a kadmia. Zdroj [6] uvádza, že celkový obsah zinku v salmiakovom stere je približne 40 %.
V súčasnosti salmiakový ster, ktorý je relatívne bohatým zdrojom zinku končí na skládke nebezpečného odpadu bez jeho ďalšieho spracovania. Je dôležité zaoberať sa možnosťami spracovania tohto odpadu.
V súčasnosti na Slovensku tento spôsob zinkovania realizuje len jedna spoločnosť, ktorá ročne vyprodukuje približne 30 ton salmiakového steru. V Českej republike túto technológiu zinkovania využívajú tri spoločnosti.
V minulosti technológia mokrého kusového žiarového zinkovania bola oveľa viacej využívaná. S tým súvisela aj väčšia tvorba salmiakových sterov.
Spracovaním salmiakového steru sa zaoberal Raymond J. Kepfer [10] ktorý sa vo svojej štúdií zameral na získavanie zložiek nachádzajúcich sa v salmiakovom stere. Cieľom bolo získanie tuhých zvyškov bez amoniakových zlúčenín a roztokov obsahujúcich Zn-Cl2-NH4Cl t.j. podvojnú soľ (ZnCl2.2NH4Cl), ktorú možno použiť ako tavidlo v procese suchého zinkovania. Tieto produkty boli produkované prídavkom NH4OH. Salmiakový ster bol rozpustený vo vode, do ktorej bol následne pridaný hydroxid amónny. Zmes bola mechanicky miešaná po dobu 30 min. pri teplote 48,8 °C. Následne bol roztok prefiltrovaný. Extrakčný roztok bol neutralizovaný HCl pred odparovaním a kryštalizáciou. Výsledkom bol produkt ZnCl2.3NH4Cl. Z filtračného koláča bol mechanicky oddelený kovový zinok. Zvyšok bol rozpustený v HCl za vzniku ZnCl2.
Ďalší autor Sagara M. [11] spracovával salmiakový ster pomocou elektrolýzy z roztavených soľných tavenín čoho výsledkom bol zisk kovového zinku. Sledované bolo chemické zloženie a elektrochemické vlastnosti salmiakového steru. Salmiakový ster obsahoval ZnCl2, Zn(NH3)Cl2 a ZnO.ZnCl2. V experimente bolo použité 500 g opotrebovaného tavidla, do ktorého bolo pridané 75 – 100 g NaCl a 50 – 100 g NH4Cl ako neutralizačná soľ. Takto pripravená zmes bola ohrievaná 2 hodiny pri 550 °C. Na elektrolýzu bola použitá grafitová anóda, katódu tvoril roztavený zinok. Elektrolýza prebiehala pri 500 °C, prúdovej hustote Dk = 4,5 – 5 A/cm2 s napätím článku 6 – 8 V. Dosiahnutá katódová účinnosť bola max 94 %.
Autori Kunhalmi [7] a Krištofová [8] vo svojich publikáciách uvádzajú spracovanie salmiakového steru hydrometalurgickým spôsobom. Proces pozostáva z nasledovných krokov: salmiakový ster sa lúhoval v horúcej vode. Roztok sa následne prefiltroval čím sa získal výluh a lúženec. Výluh obsahoval NH4 a ZnCl2. Lúženec obsahoval Zn, ZnO ale aj Fe2O3 ako nečistotu. Nasledovalo oddelené spracovanie lúženca a výluhu. Spracovanie výluhu pozostávalo v zahusťovaní v odparovacích zariadeniach, čím sa získal roztok s obsahom ZnCl2, ktorý je možné opätovne použiť v chemickom priemysle. Vykryštalizovaný NH4Cl možno opätovne použiť v procese žiarového zinkovania. Spracovanie lúženca pozostávalo zo sušenia, drvenia a triedenia. Triedením sa získali dve frakcie hrubozrnná obsahujúca kovový zinok a jemnozrnná frakcia, ktorú možno súčasne spracovať so zinkovým popolom.
EXPERIMENTÁLNA ČASŤ
Materiál a metodika experimentov
Na experimentálne účely bol poskytnutý materiál salmiakového steru zo Slovenskej prevádzky. Dodaný materiál mal nepravidelný tvar, preto bolo potrebné upraviť jeho zrnitosť pomocou úpravníckych metód (drvenie, mletie). Pre získanie reprezentatívnej vzorky sa pomletý ster homogenizoval nakoľko ide o heterogénni odpad. Po homogenizovaní nasledovalo a kvartovanie. Reprezentatívna vzorka steru bola podrobená chemickej analýze metódou atómovej absorpčnej spektroskopie (AAS) s cieľom kvantitatívneho stanovenia prvkov. Výsledky chemickej analýzy sú zobrazené v Tab. 1.
Tab. 1 – Chemické zloženie salmiakového steru metódou AAS
| Prvok | Zn | Cl- | Fe | Al | Si | Pb |
| Množstvo [%] | 47 | 23 | 0,03 | 0,12 | - | - |
V ďalšom kroku bol salmiakový ster pozorovaný svetelným makroskopom typu Leica Wild M3Z. Pozorovanie sa uskutočnilo pri 25 °C, normálnom atmosférickom tlaku 0,1 MPa a 60% vzdušnej vlhkosti. Z uvedeného záznamu (Obr. 3) možno konštatovať, že dodaný materiál sa vyznačuje vysokými hygroskopickými vlastnosťami, pretože už v priebehu 16 sekúnd salmiakový ster pohlcoval vzdušnú vlhkosť ako je to zrejmé zo záznamu.
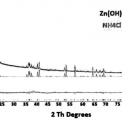
S cieľom zistenia fázového zloženia sa reprezentatívna vzorka salmiakového steru podrobila kvalitatívnej a kvantitatívnej RTG difrakčnej analýze. Výsledky RTG difrakčnej analýzy zobrazuje obr. 4.
Výsledkom RTG difrakčnej analýzy steru bolo zistenie, že zinok je prítomný vo fázach: Zn(OH)Cl a NH4Cl.
Lúhovanie salmiakového steru
Experimenty boli uskutočnené v sklenenej kadičke ponorenej vo vodnom kúpeli pri teplote 20 °C za stáleho miešania. Ako lúhovacie médium bola použitá destilovaná voda a 0,25 M; 0,5 M; 1 M a 2 M kyselina chlorovodíková. Doba lúhovania bola konštantná 90 min. Sledoval sa rôzny pomer K:P (kvapalná : pevná fáza) – 80:1; 40:1; 20:1. V časových intervaloch1, 5, 10, 15, 20, 25, 30, 60 a 90 min. boli odoberané kvapalné vzorky s cieľom stanovenia zinku metódou AAS.
Výsledky a diskusia
Kinetické krivky výťažnosti zinku v destilovanej vode pri 20 °C, a pomeroch K:P = 80:1, 40:1, 20:1, sú zobrazené na obr. 5. Kinetické krivky výťažnosti zinku v 0,25 M; 0,5 M; 1 M a 2 M HCl, pri 20 °C a daných pomeroch K:P sú uvedené na obr. 6, 7, 8, 9.
Cieľom experimentov bolo zistiť vplyv pomeru K:P na výťažnosť zinku v prostredí destilovanej vody pri teplote 20 °C. Z výsledkov výťažnosti zinku možno konštatovať Obr. 5), že optimálnym pomerom K:P v prostredí destilovanej vody je pomer 80:1. Najvyššia výťažnosť zinku (65 %) bola dosiahnutá pri tomto pomere v priebehu 5–10 min. lúhovania.
Vyššia výťažnosť zinku bola dosiahnutá v 0,25 M HCl. Pri použití 0,25 M HCl ako lúhovacieho činidla bola dosiahnutá takmer 100% výťažnosť zinku v priebehu prvých 5 min. pri K:P = 40:1 (obr. 6). S rastúcou dobou lúhovania výťažnosť zinku mierne klesala.
Pri lúhovaní salmiakového steru v 0,5 M HCl (Obr. 7) už v prvej minúte lúhovania bola dosiahnutá 82 % výťažnosť zinku pri pomere K:P = 20:1. Avšak táto výťažnosť prudko klesla v piatej minúte (69 %), s predlžujúcou sa dobou lúhovania nastalo ustálenie procesu.
Z výsledkov lúhovania steru v prostredí 1 M HCl a 20 °C (obr. 8) možno konštatovať, že optimálnym pomerom K:P v tomto prostredí je K:P = 80:1. Krivky výťažnosti zobrazujú, že najvyššia dosiahnutá výťažnosť zinku bola takmer 100 % priebehu 1 – 5 min.
Kinetické krivky výťažnosti zinku v prostredí 2 M HCl a 20 °C sú zobrazené na Obr. 9. Z týchto kriviek vyplýva, že najvyššia výťažnosť zinku do roztoku (takmer 100 %) bola dosiahnutá pri pomere K:P = 80:1 v prvej minúte. S predlžujúcou sa dobou lúhovania výťažnosť zinku mierne klesala.
ZÁVER
Predložená práca stručne opisuje tvorbu salmiakového steru vznikajúceho len pri mokrom kusovom žiarovom zinkovaní. Tento odpad podľa Vyhlášky MŽP SR 284/2001 Z.z., ktorou sa ustanovuje Katalóg odpadov sa zaraďuje medzi „nebezpečný odpad“. V súčasnosti končí na skládke odpadov aj napriek skutočnosti, že obsahuje približne 40 % celkového zinku.
Príspevok sa tiež zameral na možné spôsoby spracovania salmiakového steru.
V experimentálnej časti bol salmiakový ster podrobený hydrometalurgickému spracovaniu – lúhovaniu. Cieľom bolo zistiť vhodné podmienky vylúhovania zinku do roztoku s najvyššou výťažnosťou. Z dosiahnutých výsledkov vylúhovania zinku do roztoku je zrejmé, že:
- najvyššia výťažnosť Zn v destilovanej vode bola dosiahnutá pri pomere K:P = 80:1, kde v priebehu prvých 5 – 10 min. lúhovania sa dosiahla 65% výťažnosť,
- takmer 100% výťažnosť Zn bola dosiahnutá v 0,25 M HCl už v priebehu prvých 5 min. a pomere K:P = 40:1,
- 82% výťažnosť Zn v 0,5M HCl bola dosiahnutá pri pomere K:P = 20:1 v prvej minúte lúhovania,
- takmer 100% výťažnosti Zn boli dosiahnuté v 1M HCl aj v 2 M HCl v priebehu prvých piatich minútach pri rovnakom pomere K:P = 80:1.
Experimentálne štúdium procesov lúhovania je potrebné rozšíriť o ďalšie experimenty, v ktorých sa bude sledovať vplyv teploty na prevod zinku do roztoku.
Táto práca bola plne podporovaná grantom zo Slovenskej národnej grantovej agentúry v rámci projektu VEGA 1/0235/12.
LITERATURA:
[1] Vyhláška MŽP SR 284/2001 Z. z., Katalóg odpadov, <http://www.zakon.sk/>
[2] The Hot - Dip Galvanizing Process. Surface Preparation. <http://www.galvanizeit.org/about-hot-dip-galvanizing/what-is-hot-dip-galvanizing/hdg-process>
[3] WILFRED SPRANG. Technologie šetříci životní prostředí čelí legislativie EU v průmyslu žárového zinkování, 11. konference žárového zinkování, Nové Město na Moravě., str. 48 – 54
[4] MARDER.A.R. The metallurgy of zinc - coated steel. In: Progres in Materials Science,45, 2000, str. 191–271
[5] Hot - Dip Galvanizing. <http://www.zinc.org/info/hot_dip_galvanizing>
[6] Zaclon. Incorporated Galvanizing wet. <http://www.zaclon.com/pdf/zaclon_galvanizing_handbook.pdf>
[7] KUNHALMI G., Hutníctvo druhotných neželezných kovov, Edičné stredisko VŠT Košice, 1. Vydanie, 1984, s. 136, 85-632-84
[8] KRIŠTOFOVÁ D., Recyklace neželezných kovů. Ostrava, 2003, s. 24-26, ISBN 80-248-0485-9
[9] SJOUKES, F. Chemical reactions in fluxes for hot dip galvaniznig.,1990, str. 12-13
[10] RAYMOND J.K., Zinc ammonium chloride fluxes. United states patent office 2,127,564. <http://www.ip.com/pat/US2127564>
[11] SAGARA M..Electrolytic recovery of metallic zinc from the waste flux in the galvanizing process. <https://ds.lib.kyutech.ac.jp/dspace/handle/10228/3656>









![Obr. 1 – Prierez napeneným tavidlom a roztaveným zinkom [6]](/PublicFiles/UserFiles/image/K/2013/K613/122x122_piroskova01.jpg)
![Obr. 2 – Fázový diagram NH4Cl : ZnCl2 [6]](/PublicFiles/UserFiles/image/K/2013/K613/122x122_piroskova02.jpg)